|
|
Elementos Químicos |
|
ELEMENTOS QUÍMICOS |
|
Configuración Electrónica
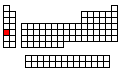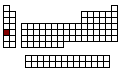
Propiedades Es un sólido blanco plateado y muy blando. Después del cesio, es el más activo de los metales alcalinos. En general, el comportamiento químico del rubidio se parece al del sodio y del potasio. Valores de las Propiedades
Empaña inmediatamente por exposición al aire y arde espontáneamente formando óxido de rubidio. Reacciona violentamente con el agua produciendo hidrógeno que arde inmediatamente después de formado. Resumen de Reactividad
|
Momento lineal | La Luz | Cinemática | Gases | Geografía | Clima | Moléculas 3D | Formularios | Catálogo Educaplus © 1996-2024, www.educaplus.org
 Menú Educaplus
Menú Educaplus