|
|
Elementos Químicos |
|
ELEMENTOS QUÍMICOS |
|
Configuración Electrónica
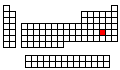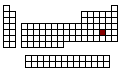
Propiedades Es un sólido gris plateado, quebradizo y de carácter semimetálico. Tiene una baja conductividad eléctrica metaloide blanco. El teluro es un elemento relativamente estable, insoluble en agua y ácido clorhídrico pero soluble en el ácido nítrico y agua regia. Valores de las Propiedades
El teluro reacciona con exceso de cloro para formar dicloruro de teluro, TeCl2 , y tetracloruro de teluro, TeCl4. Es oxidado por el ácido nítrico produciendo dióxido de teluro, TeO2 , y por el ácido crómico para producir ácido telúrico, H2TeO4. En combinación con el hidrógeno o ciertos metales, forma telururos como telururo de hidrógeno, H2Te, y telururo de sodio, Na2Te. Resumen de Reactividad
|
Momento lineal | La Luz | Cinemática | Gases | Geografía | Clima | Moléculas 3D | Formularios | Catálogo Educaplus © 1996-2024, www.educaplus.org
 Menú Educaplus
Menú Educaplus