|
|
Elementos Químicos |
|
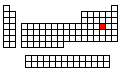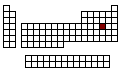
ELEMENTOS QUÍMICOS |
|
Configuración Electrónica
Propiedades Se presenta en varias formas alotrópicas: como plovo de color rojo ladrillo, como sólido amorfo vítreo de color castaño oscuro, como cristales monoclínicos rojos y como cristales brillantes de color gris. Esta última, llamada selenio gris, tiene un débil carácter metálico, conduce el calor y su conductvidad eléctrica aumenta con la iluminación. Valores de las Propiedades
Químicamente, el selenio se parece bastante al azufre y algo menos al teluro. Reacciona con muchos elementos y con ácidos y bases. Forma ácido selenioso (H2SeO3) y ácido selénico (H2SeO4), llamándose selenitos y seleniatos sus sales respectivas. Resumen de Reactividad
|
Momento lineal | La Luz | Cinemática | Gases | Geografía | Clima | Moléculas 3D | Formularios | Catálogo Educaplus © 1996-2024, www.educaplus.org
 Menú Educaplus
Menú Educaplus