



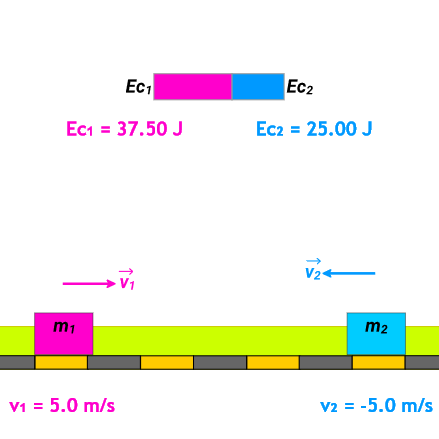


Pulsa en el demonio para activar/desactivar la puerta e intenta separar las bolas rojas de las azules.
En uno de los capítulos de su libro Theory of Heat, publicado en 1871, J. C. Maxwell planteaba un experimento mental pensado para ilustrar las limitaciones de la segunda ley de la Termodinámica que puede resumir asi:
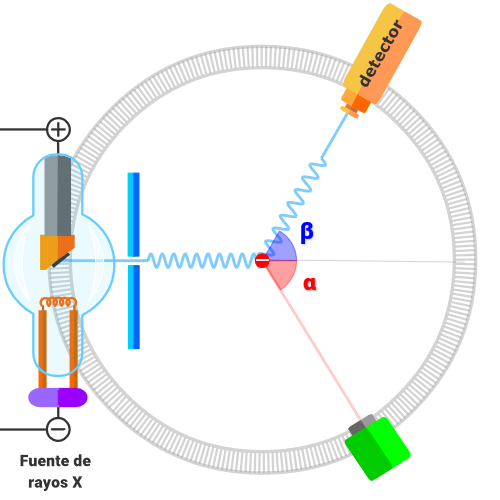
Supongamos que tenemos un recipiente con muchas moléculas, a distintas velocidades, moviendose en todas direcciones. Este recipiente está dividido en dos partes por una "puerta" y hay un ser diminuto, que abre y cierra la puerta, dejando pasar las moléculas más rápidas hacia un lado y las más lentas hacia el otro. De esta forma, se conseguirá elevar la temperatura de un lado y bajar la del otro sin efectuar trabajo, violando así la segunda ley de la termodinámica.
El nombre de Demonio de Maxwell fue puesto por William Thomson en 1874 en su artículo Kinetic Theory of the Dissipation of Energy.
Veamos qué pasa con las dos primeras leyes de la Termodinámica cuando opera el demonio:
La segunda ley exige que la entropía del demonio se incremente en una cantidad mayor o igual a la disminución en la entropía del gas.
La primera ley implica que las energías del demonio y del gas no deben cambiar (sistema aislado)
Por lo tanto, el demonio debe aumentar su entropía manteniendo la energía fija. Pero si el demonio aumenta su entropía infinitamente se volverá tan desordenado que será incapaz de llevar a cabo sus tareas.
Necesitaríamos periódicamente devolver al demonio a su estado inicial y para ello deberíamos contar con un reservorio en el que el demonio pudiera ir depositando su exceso de entropía y necesitamos también una fuente de trabajo, que le entregue energía al demonio a entropía constante.
En resumen:
1. La entropía del demonio se incrementa cuando disminuye la entropía del gas.
2. El demonio no puede ser devuelto a su estado inicial sin intercambiar energía con fuentes externas.
Etiquetas: Bachillerato HTML5 RF
